ალცჰაიმერის დაავადება, ხანდაზმულებში ყველაზე გავრცელებული დაავადება, ადამიანების უმეტესობას აწუხებს.
ალცჰაიმერის დაავადების მკურნალობის ერთ-ერთი გამოწვევა ის არის, რომ თერაპიული პრეპარატების ტვინის ქსოვილში მიწოდება შეზღუდულია ჰემატოენცეფალური ბარიერით. კვლევამ აჩვენა, რომ მაგნიტურ-რეზონანსული ტომოგრაფიით კონტროლირებად დაბალი ინტენსივობის ფოკუსირებულ ულტრაბგერით შესაძლებელია ჰემატოენცეფალური ბარიერის შექცევადად გახსნა ალცჰაიმერის დაავადების ან სხვა ნევროლოგიური დარღვევების მქონე პაციენტებში, მათ შორის პარკინსონის დაავადების, ტვინის სიმსივნეების და ამიოტროფიული გვერდითი სკლეროზის დროს.
დასავლეთ ვირჯინიის უნივერსიტეტის როკფელერის ნეირომეცნიერების ინსტიტუტში ჩატარებულმა ცოტა ხნის წინ ჩატარებულმა მცირე მასშტაბიანმა კვლევამ აჩვენა, რომ ალცჰაიმერის დაავადების მქონე პაციენტებმა, რომლებიც ადუკანუმაბის ინფუზიას ფოკუსირებულ ულტრაბგერასთან ერთად იღებდნენ, დროებით გახსნეს ჰემატოენცეფალური ბარიერი, რამაც მნიშვნელოვნად შეამცირა ტვინის ამილოიდ ბეტა (Aβ) დატვირთვა კვლევის დროს. კვლევამ შესაძლოა ახალი გზები გახსნას ტვინის დარღვევების მკურნალობისთვის.
ჰემატოენცეფალური ბარიერი იცავს ტვინს მავნე ნივთიერებებისგან და ამავდროულად საშუალებას აძლევს აუცილებელ საკვებ ნივთიერებებს გაიარონ. თუმცა, ჰემატოენცეფალური ბარიერი ასევე ხელს უშლის თერაპიული პრეპარატების ტვინში მიწოდებას, რაც განსაკუთრებით მწვავე გამოწვევაა ალცჰაიმერის დაავადების მკურნალობისას. მსოფლიოს დაბერებასთან ერთად, ალცჰაიმერის დაავადებით დაავადებული ადამიანების რიცხვი წლიდან წლამდე იზრდება და მისი მკურნალობის ვარიანტები შეზღუდულია, რაც მძიმე ტვირთად აწვება ჯანდაცვას. ადუკანუმაბი არის ამილოიდ ბეტა (Aβ)-შემაკავშირებელი მონოკლონური ანტისხეული, რომელიც დამტკიცებულია აშშ-ის სურსათისა და წამლის ადმინისტრაციის (FDA) მიერ ალცჰაიმერის დაავადების სამკურნალოდ, მაგრამ მისი შეღწევა ჰემატოენცეფალურ ბარიერში შეზღუდულია.
ფოკუსირებული ულტრაბგერა წარმოქმნის მექანიკურ ტალღებს, რომლებიც იწვევს რხევებს შეკუმშვასა და განზავებას შორის. სისხლში შეყვანისას და ულტრაბგერითი ველის ზემოქმედებისას, ბუშტები იკუმშება და ფართოვდება მიმდებარე ქსოვილსა და სისხლზე მეტად. ეს რხევები ქმნის მექანიკურ სტრესს სისხლძარღვის კედელზე, რაც იწვევს ენდოთელურ უჯრედებს შორის მჭიდრო კავშირების გაჭიმვას და გახსნას (სურათი ქვემოთ). შედეგად, ირღვევა ჰემატოენცეფალური ბარიერის მთლიანობა, რაც მოლეკულებს საშუალებას აძლევს დიფუზირდნენ ტვინში. ჰემატოენცეფალური ბარიერი თავისით აღდგება დაახლოებით ექვს საათში.
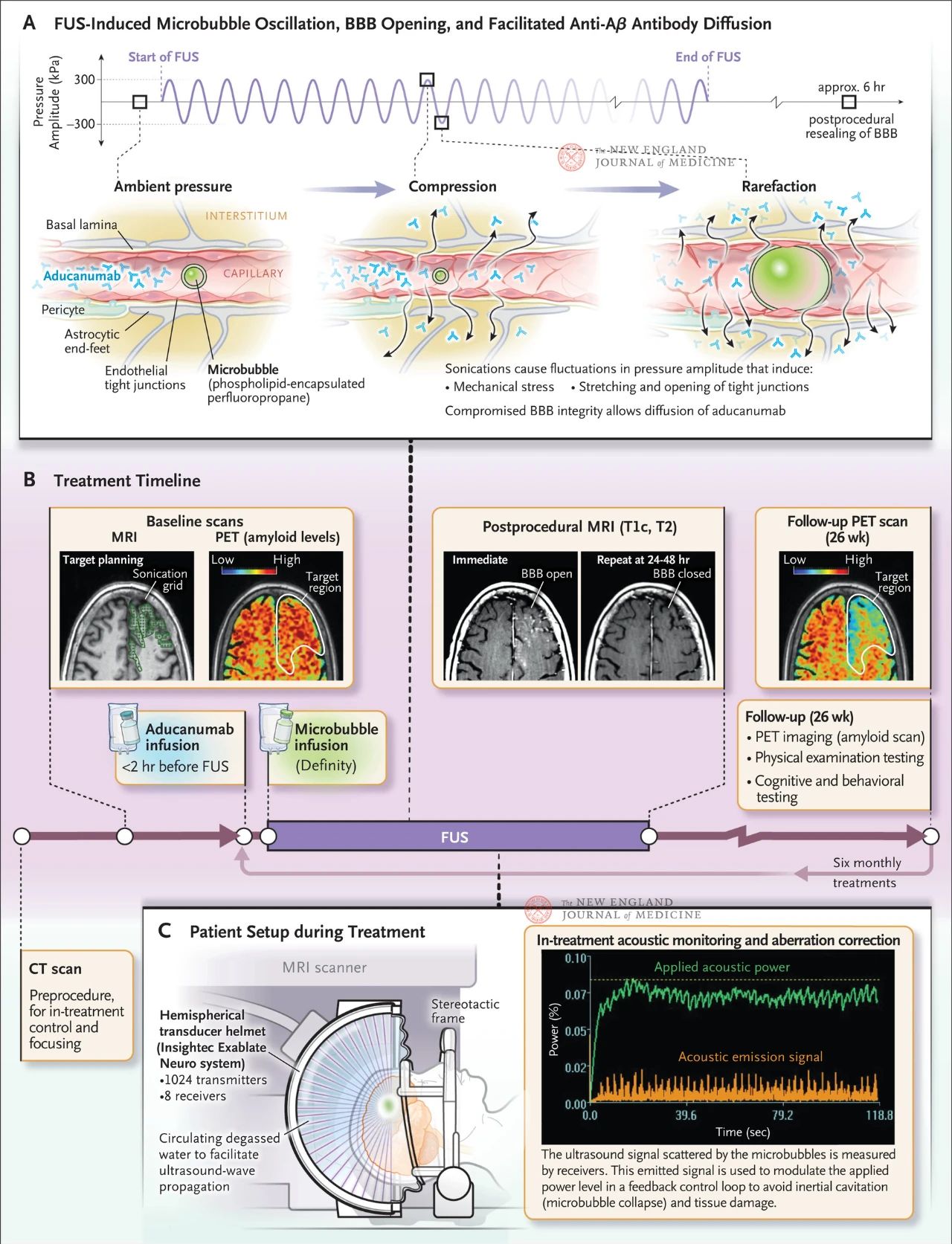
ნახაზზე ნაჩვენებია მიმართული ულტრაბგერის გავლენა კაპილარების კედლებზე, როდესაც სისხლძარღვებში მიკრომეტრის ზომის ბუშტებია. გაზის მაღალი შეკუმშვის გამო, ბუშტები იკუმშება და ფართოვდება მიმდებარე ქსოვილზე მეტად, რაც იწვევს მექანიკურ სტრესს ენდოთელურ უჯრედებზე. ეს პროცესი იწვევს მჭიდრო კავშირების გახსნას და ასევე შეიძლება გამოიწვიოს ასტროციტების დაბოლოებების სისხლძარღვის კედლიდან ჩამოვარდნა, რაც საფრთხეს უქმნის ჰემატოენცეფალურ ბარიერს და ხელს უწყობს ანტისხეულების დიფუზიას. გარდა ამისა, ფოკუსირებული ულტრაბგერის ზემოქმედების ქვეშ მყოფმა ენდოთელური უჯრედებმა გააძლიერეს მათი აქტიური ვაკუოლური ტრანსპორტირების აქტივობა და დათრგუნეს გამოდევნის ტუმბოს ფუნქცია, რითაც შეამცირეს ტვინის ანტისხეულების კლირენსი. ნახაზ B გვიჩვენებს მკურნალობის გრაფიკს, რომელიც მოიცავს კომპიუტერულ ტომოგრაფიას (CT) და მაგნიტურ-რეზონანსულ ტომოგრაფიას (MRI) ულტრაბგერითი მკურნალობის გეგმის შესამუშავებლად, 18F-ფლუბიტაბანის პოზიტრონულ-ემისიური ტომოგრაფიას (PET) საწყის ეტაპზე, ანტისხეულების ინფუზიას ფოკუსირებულ ულტრაბგერით მკურნალობამდე და მიკროვეზიკულურ ინფუზიას მკურნალობის დროს, და მიკროვეზიკულური გაფანტვის ულტრაბგერითი სიგნალების აკუსტიკურ მონიტორინგს, რომლებიც გამოიყენება მკურნალობის კონტროლისთვის. ფოკუსირებული ულტრაბგერითი მკურნალობის შემდეგ მიღებულ სურათებს შორის იყო T1-შეწონილი კონტრასტით გაძლიერებული მაგნიტურ-რეზონანსული ტომოგრაფია, რომელმაც აჩვენა, რომ ჰემატოენცეფალური ბარიერი ღია იყო ულტრაბგერით დამუშავებულ არეალში. ფოკუსირებული ულტრაბგერითი მკურნალობის 24-48 საათის შემდეგ იმავე არეალის სურათებმა აჩვენა ჰემატოენცეფალური ბარიერის სრული შეხორცება. 26 კვირის შემდეგ, ერთ-ერთი პაციენტის დაკვირვების დროს ჩატარებულმა 18F-ფლუბიტაბანის პოზიტრონ-ემისიური ტომოგრაფიამ აჩვენა Aβ დონის შემცირება ტვინში მკურნალობის შემდეგ. სურათი C გვიჩვენებს მაგნიტურ-რეზონანსული ტომოგრაფიით ხელმძღვანელობით ფოკუსირებული ულტრაბგერითი სისტემის სქემას მკურნალობის დროს. ნახევარსფეროსებრი გადამყვანი ჩაფხუტი შეიცავს 1000-ზე მეტ ულტრაბგერით წყაროს, რომლებიც თავს იყრიან ტვინის ერთ ფოკუსურ წერტილში მაგნიტურ-რეზონანსული ტომოგრაფიის რეალურ დროში ხელმძღვანელობის გამოყენებით.
2001 წელს, ცხოველებზე ჩატარებულმა კვლევებმა პირველად აჩვენა, რომ ფოკუსირებული ულტრაბგერითი გამოკვლევა იწვევდა ჰემატოენცეფალურ ბარიერის გახსნას, ხოლო შემდგომმა კლინიკურმა კვლევებმა აჩვენა, რომ ფოკუსირებულ ულტრაბგერას შეუძლია გააძლიეროს წამლის მიწოდება და ეფექტურობა. მას შემდეგ დადგინდა, რომ ფოკუსირებულ ულტრაბგერას შეუძლია უსაფრთხოდ გახსნას ჰემატოენცეფალური ბარიერი ალცჰაიმერის დაავადების მქონე პაციენტებში, რომლებიც არ იღებენ მედიკამენტებს, და ასევე შეუძლია მიაწოდოს ანტისხეულები ძუძუს კიბოს ტვინის მეტასტაზების საწინააღმდეგოდ.
მიკრობუშტების მიწოდების პროცესი
მიკრობუშტები ულტრაბგერითი კონტრასტული საშუალებაა, რომელიც ჩვეულებრივ გამოიყენება სისხლის ნაკადისა და სისხლძარღვების დასაკვირვებლად ულტრაბგერითი დიაგნოსტიკის დროს. ულტრაბგერითი თერაპიის დროს ინტრავენურად შეჰყავდათ ოქტაფტორპროპანის ფოსფოლიპიდებით დაფარული არაპიროგენული ბუშტუკოვანი სუსპენზია (სურათი 1B). მიკრობუშტები მაღალპოლიდისპერსულია, დიამეტრით 1 მკმ-ზე ნაკლებიდან 10 მკმ-ზე მეტამდე. ოქტაფტორპროპანი სტაბილური აირია, რომელიც არ მეტაბოლიზდება და მისი გამოყოფა ფილტვების მეშვეობით შეიძლება. ლიპიდური გარსი, რომელიც ბუშტებს ახვევს და ასტაბილურებს, შედგება სამი ბუნებრივი ადამიანის ლიპიდისგან, რომლებიც მეტაბოლიზდება ენდოგენური ფოსფოლიპიდების მსგავსად.
ფოკუსირებული ულტრაბგერის გენერირება
ფოკუსირებული ულტრაბგერა გენერირდება ნახევარსფეროსებრი გადამყვანი ჩაფხუტით, რომელიც პაციენტის თავს აკრავს (სურათი 1C). ჩაფხუტი აღჭურვილია 1024 დამოუკიდებლად კონტროლირებადი ულტრაბგერითი წყაროთი, რომლებიც ბუნებრივად ფოკუსირებულია ნახევარსფეროს ცენტრში. ეს ულტრაბგერითი წყაროები იმართება სინუსოიდური რადიოსიხშირული ძაბვებით და გამოყოფენ ულტრაბგერით ტალღებს, რომლებსაც მაგნიტურ-რეზონანსული ტომოგრაფია მართავს. პაციენტი ატარებს ჩაფხუტს და დეგაზირებული წყალი თავის გარშემო ცირკულირებს ულტრაბგერის გადაცემის გასაადვილებლად. ულტრაბგერა კანსა და თავის ქალაში გადის ტვინის სამიზნე ნაწილამდე.
თავის ქალას სისქისა და სიმკვრივის ცვლილებები გავლენას მოახდენს ულტრაბგერის გავრცელებაზე, რაც გამოიწვევს ულტრაბგერით დაზიანებამდე მისასვლელად დროის ოდნავ განსხვავებულ ცვლილებას. ამ დამახინჯების გამოსწორება შესაძლებელია მაღალი გარჩევადობის კომპიუტერული ტომოგრაფიის მონაცემების მიღებით, რათა მივიღოთ ინფორმაცია თავის ქალის ფორმის, სისქისა და სიმკვრივის შესახებ. კომპიუტერული სიმულაციის მოდელს შეუძლია გამოთვალოს თითოეული წამყვანი სიგნალის კომპენსირებული ფაზური ცვლა მკვეთრი ფოკუსის აღსადგენად. რადიოსიხშირული სიგნალის ფაზის კონტროლით, ულტრაბგერა შეიძლება ელექტრონულად ფოკუსირდეს და განთავსდეს ქსოვილის დიდი რაოდენობით დასაფარად ულტრაბგერითი წყაროს მასივის გადაადგილების გარეშე. სამიზნე ქსოვილის მდებარეობა განისაზღვრება თავის მაგნიტურ-რეზონანსული ტომოგრაფიით ჩაფხუტის ტარებისას. სამიზნე მოცულობა ივსება ულტრაბგერითი საყრდენი წერტილების სამგანზომილებიანი ბადით, რომლებიც ასხივებენ ულტრაბგერით ტალღებს თითოეულ საყრდენ წერტილში 5-10 ms-ის განმავლობაში, მეორდება ყოველ 3 წამში. ულტრაბგერითი სიმძლავრე თანდათან იზრდება სასურველი ბუშტუკების გაფანტვის სიგნალის აღმოჩენამდე და შემდეგ შენარჩუნებულია 120 წამის განმავლობაში. ეს პროცესი მეორდება სხვა ბადეებზე მანამ, სანამ სამიზნე მოცულობა სრულად არ დაიფარება.
ჰემატოენცეფალური ბარიერის გასახსნელად საჭიროა ბგერითი ტალღების ამპლიტუდამ გადააჭარბოს გარკვეულ ზღვარს, რომლის მიღმაც ბარიერის გამტარიანობა იზრდება წნევის ამპლიტუდის ზრდასთან ერთად ქსოვილის დაზიანებამდე, რაც ვლინდება ერითროციტების ეგზოსმოსით, სისხლდენით, აპოპტოზით და ნეკროზით, რომლებიც ხშირად ასოცირდება ბუშტუკების კოლაფსთან (ე.წ. ინერციული კავიტაცია). ზღვარი დამოკიდებულია მიკრობუშტების ზომასა და გარსის მასალაზე. მიკრობუშტების მიერ გაფანტული ულტრაბგერითი სიგნალების აღმოჩენითა და ინტერპრეტაციით, შესაძლებელია ზემოქმედების უსაფრთხო დიაპაზონში შენარჩუნება.
ულტრაბგერითი მკურნალობის შემდეგ, სამიზნე ადგილას ჰემატოენცეფალური ბარიერის გახსნის დასადგენად გამოყენებული იქნა T1-შეწონილი მაგნიტურ-რეზონანსული ტომოგრაფია კონტრასტული ნივთიერებით, ხოლო ექსტრავაზაციის ან სისხლდენის დასადასტურებლად გამოყენებული იქნა T2-შეწონილი გამოსახულებები. ეს დაკვირვებები საჭიროების შემთხვევაში სხვა მკურნალობის მეთოდების კორექტირების სახელმძღვანელოს წარმოადგენს.
თერაპიული ეფექტის შეფასება და პერსპექტივა
მკვლევრებმა ტვინის Aβ დატვირთვაზე მკურნალობის ეფექტი რაოდენობრივად განსაზღვრეს მკურნალობამდე და მკურნალობამდე და მის შემდეგ ჩატარებული 18F-ფლუბიტაბანის პოზიტრონ-ემისიური ტომოგრაფიის შედარებით, რათა შეფასებულიყო Aβ მოცულობის სხვაობა დამუშავებულ უბანსა და საპირისპირო მხარეს მდებარე A მსგავს უბანს შორის. იმავე ჯგუფის მიერ ჩატარებულმა წინა კვლევებმა აჩვენა, რომ ულტრაბგერითი ფოკუსირება უბრალოდ Aβ დონის უმნიშვნელოდ შემცირებას უწყობს ხელს. ამ კვლევაში დაფიქსირებული შემცირება კიდევ უფრო დიდი იყო, ვიდრე წინა კვლევებში.
მომავალში, მკურნალობის ტვინის ორივე მხარეს გაფართოება კრიტიკულად მნიშვნელოვანი იქნება დაავადების პროგრესირების შეფერხების ეფექტურობის შესაფასებლად. გარდა ამისა, საჭიროა მეტი კვლევა გრძელვადიანი უსაფრთხოებისა და ეფექტურობის დასადგენად და უფრო ფართო ხელმისაწვდომობისთვის აუცილებელია ეკონომიური თერაპიული მოწყობილობების შემუშავება, რომლებიც არ ეყრდნობიან ონლაინ მაგნიტურ-რეზონანსული ტომოგრაფიის ხელმძღვანელობას. მიუხედავად ამისა, აღმოჩენებმა ოპტიმიზმი გააჩინა, რომ მკურნალობა და Aβ-ს გამწმენდი პრეპარატები საბოლოოდ შეანელებს ალცჰაიმერის პროგრესირებას.
გამოქვეყნების დრო: 2024 წლის 6 იანვარი